
- Autor Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:14.
- Zadnja izmjena 2025-01-22 15:53.
Aplikacija za klinička ispitivanja ( CTA ) je zahtjev/podnošenje nadležnom državnom. Regulatorno Autoritet(a) za odobrenje za sprovođenje kliničkog ispitivanja u određenoj zemlji. Primjeri. podneske nadležnim nacionalnim Regulatorno Vlasti mogu uključivati, ali nisu ograničene na: 1.
Što se toga tiče, šta je CTA u kliničkim istraživanjima?
A Kliničkim ispitivanjima Sporazum ( CTA ) je pravno obavezujući ugovor koji upravlja odnosom između sponzora koji može pružiti studija lijek ili uređaj, finansijsku podršku i/ili vlasničke informacije i instituciju koja može pružati podatke i/ili rezultate, objavljivanje, unos u daljnje
Slično tome, ko odobrava klinička ispitivanja u UK? Suđenje autorizacija Sve kliničkim ispitivanjima lijekova i studija o medicinskim uređajima također moraju biti odobreni od strane organizacije koja se zove Regulatorna agencija za lijekove i zdravstvene proizvode (MHRA). Ovo se zove Kliničkim ispitivanjima Autorizacija (CTA).
Nakon toga, postavlja se pitanje šta je CTA u farmaceutskim proizvodima?
Odobrenja za klinička ispitivanja ( CTA ); (IND) Postupak uključuje dobijanje EudraCT broja od Evropske agencije za lijekove (EMA) i podnošenje zahtjeva za odobrenje kliničkog ispitivanja ( CTA ) nadležnom organu svake države članice u kojoj će se ispitivanje voditi.
Da li je Inds odobren?
IND nije aplikacija za marketing odobrenje . To je put kojim sponzor dobija od Uprave za hranu i lekove (FDA) izuzeće od federalnog zakona koji zabranjuje transport neodobrenih lekova preko državnih granica.
Preporučuje se:
Šta je podračun i za šta se koristi?

Podračun je odvojeni račun ugniježđen pod većim računom ili odnosom. Ovi zasebni računi mogu sadržavati podatke, korespondenciju i druge korisne informacije ili sadržavati sredstva koja se čuvaju u banci
Šta je dopis i za šta se koristi?

Memorandum (ili memorandum, što znači „podsjetnik“) se obično koristi za komuniciranje politika, procedura ili povezanih službenih poslova unutar organizacije
Šta je faktor, a šta višekratnik?
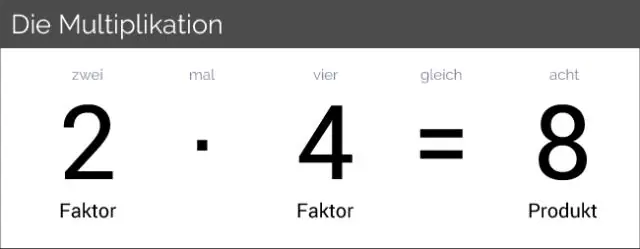
Višekratnik je broj koji se može podijeliti s drugim brojem određeni broj puta bez ostatka. Faktor je jedan od dva ili više brojeva koji dijele dati broj bez ostatka
Šta je MasterFormat Za šta se koristi?

Organizirajte svoje građevinske specifikacije i informacije o projektu MasterFormat je sistem kodiranja za organiziranje građevinskih dokumenata, ugovora, specifikacija dizajna i operativnih priručnika. Koristi specifične brojeve i povezane naslove koji čine univerzalni sistem indeksiranja
Šta je CTA u farmaciji?

Odobrenja za klinička ispitivanja (CTA); (IND) Postupak uključuje dobijanje EudraCT broja od Evropske agencije za lijekove (EMA) i podnošenje zahtjeva za odobrenje kliničkog ispitivanja (CTA) nadležnom tijelu svake države članice u kojoj će se ispitivanje provoditi
